
Лабораторная работа №2
Изучение методов определения содержания белка в сырье и готовой продукции
Определение содержания белков.
Цель работы. Овладеть методами определения содержания белков в пищевых продуктах.
Теоретическое обоснование. Белки - это высокомолекулярные органические соединения, построенные из аминокислот, соединенных между собой пептидными связями. Роль белков в организме человека чрезвычайно важна, так как они участвуют в важнейших процессах в организме. Необходимость их постоянного обновления лежит в основе обмена веществ. Белки в организме выполняют структурную (входят в состав тканей и клеток) и функциональную (ферменты, гормоны и др.) роль.
Потребление белков должно быть оптимальным, так как и недостаток, и избыток белков в пище вреден для человека. Потребность взрослого человека составляет в среднем 100 г белка в сутки. По составу белковые вещества в пище должны быть примерно на 2/3 животного происхождения и на 1/3 - растительного. Белками богаты мясо, рыба, яйца, молоко, злаковые и бобовые культуры.
Массовую долю белка в пищевых продуктах определяют различными методами:
Наиболее точным является метод Къельдаля, который заключается в окислении (сжигании) органических веществ концентрированной серной кислотой при кипячении в присутствии катализатора. Содержание белка определяют по количеству азота. Метод Къельдаля длительный и трудоемкий, требует высокой квалификации работающего.
В связи с этим широко применяются физико-химические (ускоренные) методы количественного определения белка, основанные на специфических свойствах белка:
- способности адсорбировать некоторые красители (метод Юди);
- способности пептидных связей белка образовывать комплексное окрашенное соединение с ионами меди в щелочном растворе (биуретовый);
- способности активных групп различных аминогрупп, входящих в состав полипептидной цепи белка, давать характерные реакции (метод Лоури) и др. Преимущество этих методов в том, что они отличаются достаточно высокой точностью, простотой и быстротой определения.
Оборудование и техническое оснащение лабораторной работы.
Прибор нагревательный для сжигания навесок; прибор для перегонки с каплеуловителем; колбы Къельдаля; колбы конические; цилиндры мерные; бюретки вместимостью; капельница. Мука, раствор КОН; сегнетова соль; дистиллированная вода; раствор СиSО4; СС14; раствор КОН; сульфосалициловая кислота; мерные колбы, пробки для колб; пипетки; весы; механический встряхиватель; центрифуга; фотоэлектроколориметр; фотоэлектрический нефелометр.
Содержание и порядок выполнения лабораторной работы:
Метод Къельдаля.
Навеску из гомогенной массы берут с таким расчетом, чтобы в пробе содержалось примерно 20...25 мг азота. Метод основан на сжигании органических компонентов пробы пищи в присутствии серной кислоты. Выделяющийся при этом азот улавливается серной кислотой и образуется сульфат аммония. При добавлении едкого натра выделяется аммиак, который отгоняют в раствор серной кислоты. Выделившийся аммиак определяют титрованием. Для ускорения сжигания применяют катализатор: смесь серно-кислой меди и серно-кислого натрия.
Аппаратура, материалы, реактивы. Прибор нагревательный для сжигания навесок; прибор для перегонки с каплеуловителем; колбы Къельдаля вместимостью 100 см3 с грушевидной стеклянной пробкой; колбы конические вместимостью 250 см3; цилиндры мерные на 25, 50, 100 см3; бюретки вместимостью 25 см3 с ценой деления 0,1 см3; капельница. Серная кислота плотностью 1,84 г/см3, 33 %-ный раствор гидроокиси натрия, 0,05 моль/дм3 раствор серной кислоты, смешанный индикатор (к 25 см3 0,1 %-ного раствора метиленового голубого добавляют 3 см3 0,02 %-ного спиртового раствора метилового красного), лакмусовая бумага.
Методика анализа. В колбу Къельдаля переносят навеску, которую берут на аналитических весах в лодочку из алюминиевой фольги или подпергаментной бумаги, добавляют цилиндром 20 см3 серной кислоты, вливая ее постепенно по стенкам колбы и смывая частицы продукта. В колбу добавляют катализатор (0,5 г серно-кислой меди и 7,5 г серно-кислого натрия), устанавливают ее в наклонном положении в вытяжном шкафу в нагревательный прибор, приливают 1 см3 этилового спирта. Колбу закрывают грушевидной стеклянной пробкой и осторожно нагревают. При образовании пены в первый период окисления колбу следует снять с нагревательного прибора и дать пене осесть, а затем продолжить нагревание, следя за тем, чтобы пена не попала в горло колбы. После прекращения пенообразования нагрев усиливают. Степень нагревания считают достаточной, когда кипящая кислота конденсируется в средней части горлышка колбы Къельдаля.
Время от времени содержимое колбы перемешивают, смывая частицы со стенок колбы. Нагревание продолжают до тех пор, пока жидкость не станет бесцветной (слегка голубоватой) и совершенно прозрачной. Содержимое колбы охлаждают, осторожно по стенке добавляют 50 см3 дистиллированной воды, перемешивают и охлаждают.
В коническую колбу вместимостью 250 см3 пипеткой отмеривают 40 см3 0,05 моль/дм3 серной кислоты, добавляют четыре капли индикатора, перемешивают и погружают наконечник, соединенный с холодильником, в кислоту на 1,5...2 см.
В перегонную колбу переносят содержимое колбы Къельдаля, ополаскивая ее несколько раз, 100...150 см3 дистиллированной воды, опускают красную лакмусовую бумажку и соединяют с холодильником с помощью каплеуловителя. Отмеривают цилиндром 80 см3 33 %-ного раствора гидроокиси натрия и через делительную воронку вливают его в перегонную колбу. Сразу же после добавления щелочи закрывают кран делительной воронки для предотвращения потерь аммиака. Содержимое колбы нагревают до кипения, при этом необходимо избегать пенообразования. Продолжают перегонку до тех пор, пока жидкость не станет вскипать толчками. Нагрев регулируют таким образом, чтобы продолжительность дистилляции была не менее 20 мин. Перед окончанием перегонки опускают коническую колбу так, чтобы конец наконечника оказался над поверхностью раствора серной кислоты, и продолжают перегонку еще 1...2 мин. Нагревание прекращают. В коническую колбу смывают небольшими порциями дистиллированной воды остатки раствора серной кислоты с внутренней и внешней поверхностей наконечника. Дистиллят титруют 0,1 моль/дм3 раствором гидроокиси натрия до перехода окраски из фиолетовой в зеленую.
Параллельно проводят контрольный анализ, добавив в колбу Кьельдаля вместо навески 5 см3 дистиллированной воды. Контрольный опыт проводят в каждой серии определений количества белка и при каждой замене реактивов.
Массу белка (X, г) вычисляют с точностью до третьего знака по формуле:
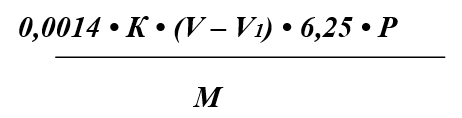
где:
0,0014 - количество азота, эквивалентное 1 см3 0,05 моль/дм3 раствора серной кислоты, г;
К - поправочный коэффициент 0,1 моль/дм3 раствора гидроокиси натрия;
V - объем 0,1 моль/дм3 раствора гидроокиси натрия, использованный на титрование 0,05 моль/дм3 раствора серной кислоты в контрольном опыте,
см3; V1 = 6,25 - коэффициент пересчета азота на белок;
Р - масса обеда или рациона, г, в рабочем опыте;
m - масса навески, г.
При исследовании проводят не менее трех определений, по результатам которых рассчитывают среднее арифметическое. Фактическое содержание белка в обеде (рационе) сравнивают с теоретическим, рассчитанным по таблицам химического состава пищевых продуктов с учетом потерь при тепловой обработке.
Определение массовой доли белка биуретовым методом.
Специфической реакцией на содержание белка является биуретовая реакция, так как ее дают полипептидные связи. Она получила свое название от производного мочевины - биурета, который образует в щелочном растворе медного купороса окрашенное комплексное соединение. Интенсивность окрашивания пропорциональна содержанию пептидных связей, а следовательно, и концентрации белка в растворе.
Биуретовую реакцию дают все белки, пептоны и полипептиды, начиная с тетрапептидов.
Эта реакция длительное время использовалась как качественная реакция на белок. В дальнейшем она стала применяться для количественного определения белка в различных объектах. Биуретовый метод применяют в различных модификациях, различающихся условиями экстрагирования белка, способами внесения биуретового реактива и техникой колориметрирования.
Ниже приводится биуретовый метод определения массовой доли белка в муке в модификации Дженнингса.
Материалы, реактивы, оборудование. Мука (объект исследования); 10 н. раствор КОН; сегнетова соль; дистиллированная вода; 4%-ный раствор СиSО4; СС14; 0,05 н. раствор КаОН; сульфосалициловая кислота; мерные колбы вместимостью 1000 см3' мерные цилиндры; конические колбы вместимостью 250-300 см3; пробки для колб; бюретки; пипетки; мерная колба вместимостью 50 см3; весы; механический встряхиватель; центрифуга; фотоэлектроколориметр; фотоэлектрический нефелометр.
Приготовление биуретового реактива. Для приготовления реактива берут 15 см3 10 н. раствора КОН и 25 г сегнетовой соли, взятой с точностью ±0,01 г, и растворяют примерно в 900 см3 дистиллированной воды в мерной колбе вместимостью 1000 см3. К этому раствору медленно добавляют при постоянном перемешивании 30 см3 4%-го раствора Си8О4, отмеренных цилиндром. Объем колбы доводят дистиллированной водой до метки.
Методика анализа. Взвешивают около 1,5 г муки с точностью ±0,001 г и помещают в сухую коническую колбу вместимостью 250-300 см3. Отмеривают под тягой цилиндром с ценой деления 0,1 см3 2 см3 четыреххлористого углерода для извлечения жира из образца и добавляют пипеткой 100 см3 биуретового реактива. Закрытую пробкой колбу встряхивают на механическом встряхивателе в течение 60 мин, а затем центрифугируют в течение 10 мин при частоте вращения 4500 мин-1. Прозрачный центрифугат помещают в кюветы фотоэлектроколориметра с толщиной слоя раствора 5 мм. Измерение оптической плотности производят при длине волны 550 нм.
По величине оптической плотности белковой вытяжки с помощью калибровочной кривой определяют массовую долю белка в навеске я (мг). Калибровочная кривая представляет собой зависимость между массой белка в навеске муки (мг) и оптической плотностью раствора.
Рассчитывают массовую долю белка (% к массе сухих веществ).
Построение калибровочной кривой. Для построения калибровочной кривой подбирают образцы муки с различной массовой долей белка в диапазоне, встречающемся в реальных условиях (от 8 до 20 %). Интервал в содержании белка в используемых образцах должен находиться в пределах не более 1 %. Количество образцов должно быть не менее 10. С увеличением их числа точность определений возрастает. Затем приведенным выше биуретовым методом определяют оптическую плотность белковых вытяжек всех образцов. При построении кривой на оси абсцисс откладывают величины оптической плотности, а на оси ординат - массовую долю белка в навеске (мг).
Определение массовой доли белка нефелометрическим методом.
Метод основан на измерении интенсивности светового потока, рассеянного твердыми или коллоидными частицами, находящимися в растворе во взвешенном состоянии. По интенсивности светорассеяния, определяемой на фотоэлектроколориметре, судят о концентрации исследуемого вещества. В настоящее время широко применяют фотоэлектрические нефелометры. Растворы высокомолекулярных соединений, например растворы белков, при определенных условиях в присутствии некоторых химических реагентов способны опалесцировать. Одним из таких реагентов является сульфосалициловая кислота. Концентрация белка в этом случае может быть определена по интенсивности опалесценции.
Продукты гидролиза белка - пептоны, аминокислоты и другие азотсодержащие вещества не опалесцируют.
Экспериментальной проверкой установлено, что нефелометрический метод с использованием сульфосалициловой кислоты отличается быстротой, высокой точностью, простотой и хорошей Корреляцией по сравнению с методом Кьельдаля.
Методика анализа. Взвешивают 0,5 г исследуемой муки с точностью ±0,001 и помещают в коническую колбу вместимостью 250-300 см3. В колбу из бюретки добавляют 50 см 0,05 н. раствора гидроксида натрия. Закрытую пробкой колбу встряхивают на механическом встряхивателе в течение 15 мин. Затем вытяжку центрифугируют в течение 10 мин при частоте вращения 6000 мин-1. Прозрачный центрифугат в количестве 5 см3 пипеткой переносят в мерную колбу на 50 см3 и содержимое колбы доводят до метки сульфосалициловой кислотой.
Получение правильных результатов при нефелометрическом методе анализа в значительной мере зависит от методики получения суспензии, в частности от порядка и скорости смешивания растворов. Поэтому после добавления сульфосалициловой кислоты колбу быстро переворачивают 2-3 раза (не более), раствор наливают в кювету с толщиной слоя 5 мм и измеряют величину оптической плотности раствора при длине волны 550 нм. Замеры следует проводить сразу после добавления кислоты, так как частицы белка быстро агрегируют.
Количество белка определяют по калибровочной кривой, построенной для этого метода и представляющей зависимость между массой белка в навеске (мг) и оптической плотностью раствора. Построение калибровочной кривой ведут аналогично описанному выше.
Запись в лабораторном журнале проводят точно так же, как в биуретовом методе. По полученным данным делают заключение о содержании белка в муке.
Требования к отчету по лабораторной работе. Лабораторные записи необходимо вести аккуратно, поэтапно, в соответствии с порядком выполнения лабораторной работы. Заносить тему, цель, материалы и оборудование, необходимые в лабораторной работе, основные этапы проведения опытов и результаты в виде тезисов, либо в табличном или графическом виде, а также с необходимыми рисунками.
Контрольные вопросы:
- Перечислите основные методы определения белка в пищевых продуктах?
- На чем основан метод Къельдаля?
- По какой формуле вычисляют количество белка Х (в г.)?
- Что такое биуретовая реакция определения белков?
- Как проводиться нефелометрический метод определения белков?