
Лабораторная работа №4
Качественное и количественное определение содержания крахмала в продовольственных продуктах
Цель работы: Изучить методы качественного определения моносахаридов и полисахаридов.
Теоретическое обоснование работы:
Свойства моносахаридов восстанавливать металлы обусловлено наличием в их структуре карбонильной группы, которая очень легко вступает в окислительно-восстановительные процессы. Особенно легко восстанавливаются такие металлы как серебро, медь, железо, висмут. Поэтому эти свойства были взяты в основу методов качественного определения моносахаридов.
Определение содержания хлеба в котлетах.
Хлеб в котлетах составляет 18-20% их массы и содержание его контролируют по количеству крахмала, которое можно определить йодометрическим, колориметрическим и цианидным методами.
Определение содержания хлеба в котлетах иодометрическим методом (арбитражный). Основа метода - гидролиз крахмала с последующим восстановлением двухвалентной меди образующимися при гидролизе редуцирующими сахарами (количество невосстановленной меди определяют йодометрическим методом в кислой среде).
Приборы и реактивы: фарфоровая чашка или химический стакан; стеклянная палочка; конические колбы вместимостью 100, 250 мл; мерные колбы вместимостью 100, 250 мл; бумажный фильтр; обратный холодильник; жидкость Фелинга (смешивают равные объемы раствора 1 (69,6 г сульфата меди растворяют в воде и доводят объем раствора до 1 л) и раствора 2 (346 г виннокислого калия-натрия и 100 г гидроксида натрия растворяют в воде и доводят объем раствора до 1 л); 10%-ный раствор соляной кислоты; 15%-ный раствор гексацианоферроата калия (желтая кровяная соль); 30%-ный раствор сульфата цинка; 25%-ный раствор серной кислоты, 0,1 М раствор тиосульфата натрия; 1%-ный раствор крахмала; 1%-ный раствор метилового красного.
Методика анализа.
- Проводят гидролиз крахмала:
- Измельченную навеску массой 5 г (взвешенную с точностью до 0,01 г) вносят в фарфоровую чашку или химический стакан, приливают 10 мл дистиллированной воды и размешивают стеклянной палочкой.
- Содержимое чашки вносят в коническую колбу вместимостью 250 мл (общее количество воды не должно превышать 40 мл), приливают 30-35 мл 10%-ного раствора соляной кислоты, присоединяют колбу к обратному холодильнику, кипятят 10 мин и охлаждают до комнатной температуры.
- После охлаждения нейтрализуют содержимое 15%-ным раствором гидроксида натрия или калия (индикатор метиловый красный) до появления слабо-желтой окраски.
- Удаляют белки:
- Нейтрализованный гидролизат вносят в мерную колбу вместимостью 250 мл, добавляют 3 мл 15%-ного раствора гексацианоферроата калия и 3 мл 30%-ного раствора сульфата цинка (для осаждения белков).
- Затем доводят объем дистиллированной водой до метки, взбалтывают и после выделения осадка гидролизат фильтруют через бумажный фильтр.
- Определяют содержание редуцирующих сахаров в гидролизате:
- В мерную колбу вместимостью 100 мл вливают 30 мл жидкости Фелинга, 25 мл гидролизата, перемешивают, кипятят 2 мин и охлаждают.
- Затем доводят объем дистиллированной водой до метки, перемешивают и дают осесть осадку оксида меди.
- 25 мл отстоявшейся ярко-синей жидкости переносят пипеткой в коническую колбу вместимостью 100-250 мл, добавляют 10 мл 30%-ного раствора йодида калия, 10 мл 25%-ного раствора серной кис лоты.
- Выделившийся йод сразу титруют 0,1 М раствором тиосульфата натрия до слабо-желтой окраски.
- Затем после появления слабо-желтой окраски добавляют 1 мл 1%-ного раствора крахмала и продолжают титровать до исчезновения синей окраски.
Одновременно проводят контрольный опыт: в мерную колбу наливают 30 мл жидкости Фелинга, 25 мл дистиллированной воды и проводят те же операции, что и с исследуемым гидролизатом.
Содержание хлеба рассчитывают по формуле:
x = (10,06 + 0,0175V)K1 * 250 * 0,9 * 100/(m0V * 10 * 48),
где:
х - содержание хлеба, %;
с - содержание глюкозы, г;
0,9 - коэффициент пересчета на крахмал;
m0 - масса навески, г;
V - объем гидролизата, взятый для кипячения, мл;
48 - коэффициент пересчета на хлеб (учитывают содержание углеводов в 100 г хлеба).
Содержание глюкозы определяют по ПРИЛОЖЕНИЮ 2 в соответствии с количеством израсходованного 0,1 М раствора тиосульфата натрия.
Количество тиосульфата натрия рассчитывают по формуле:
где:
х1 - количество тиосульфата натрия, мл;
V1 - объем 0,1 М раствора тиосульфата натрия, пошедший на титрование контрольного опыта, мл;
V2 - объем 0,1 М раствора тиосульфата натрия, пошедший на титрование испытуемого раствора, мл;
К - коэффициент пересчета на точно 0,1 М раствор тиосульфата натрия;
V3 - объем испытуемого раствора, взятый для титрования, мл.
Расхождение между параллельными определениями должно быть не более 0,5%.
Определение содержания хлеба в котлетах колориметрическим методом (ускоренный). Основа метода - гидролиз крахмала и последующее измерении интенсивности окраски раствора, возникающей при окислении редуцирующих сахаров щелочным раствором сульфата меди.
Приборы и реактивы: мерные колбы вместимостью 100 мл; стеклянный фильтр; дистиллированная вода; фотоэлектроколориметр; глюкоза х. ч.; жидкость Фелинга.
W = ((m1 - m2) * 100)/m,
Построение калибровочного графика.
- 1 г глюкозы, высушенной до постоянной массы при 70°С и взвешенной с точностью до 0,001 г, переносят количественно дистиллированной водой в мерную колбу вместимостью 100 мл, доводят объем до метки и перемешивают (основной раствор глюкозы).
- В три мерные колбы вместимостью 100 мл пипеткой вливают соответственно 10, 20, 30 мл основного раствора глюкозы, доводят каждую колбу до метки и перемешивают (получают растворы глюкозы соответственно 0,1%, 0,2% и 0,3%-ной концентрации).
- Затем в три мерные колбы вместимостью 100 мл вносят по 30 мл жидкости Фелинга и по 25 мл 0,1%-ного раствора глюкозы, содержимое колб перемешивают, кипятят 2 мин и охлаждают.
- Доводят объем раствора до метки дистиллированной водой, перемешивают, отстаивают и колориметрируют. Аналогично проводят реакцию с 0,2%-ным и 0,3%-ным растворами глюкозы, а также с дистиллированной водой.
- Для каждого раствора по полученным данным рассчитывают среднее арифметическое значение оптической плотности и по ним строят калибровочный график: на оси абсцисс откладывают концентрацию глюкозы, на оси ординат - оптическую плотность.
Методика анализа.
- Крахмал гидролизуют (методику см. выше).
- После удаления белков 25 мл раствора гидролизата вносят в мерную колбу вместимостью 100 мл, куда предварительно наливают 30 мл жидкости Фелинга, перемешивают, кипятят 2 мин и охлаждают.
- Затем доводят объем до метки дистиллированной водой и перемешивают.
- Для удаления осадка оксида меди раствор фильтруют через стеклянный фильтр № 4 и заливают в кювету фотоэлектроколориметра с расстоянием между рабочими гранями 5 мл. Интенсивность окраски измеряют при длине волны 630 нм (красный светофильтр против дистиллированной воды). Концентрацию глюкозы находят по оптической плотности на калибровочном графике (рис. 3).
Содержание хлеба рассчитывают по формуле:
где:
х - содержание хлеба, %;
а - содержание глюкозы, найденное по калибровочному графику, г;
V1 - объем гидролизата, взятый для осаждения белков, мл;
0,9 - коэффициент пересчета глюкозы на крахмал;
m0 - масса навески, г;
V2 - объем гидролизата, взятый для кипячения, мл;
48 - коэффициент пересчета крахмала на хлеб (учитывает содержание углеводов в 100 г хлеба).
Рисунок 3. Калибровочный график определения сахара по глюкозе
Определение содержания хлеба в котлетах цианидным методом. Основа метода - гидролиз крахмала и последующее восстановление гексацианоферриата калия редуцирующими сахарами гидролизата.
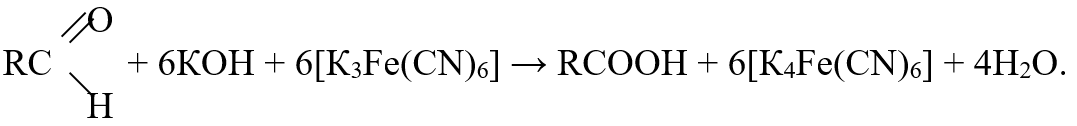
Приборы и реактивы: фарфоровая чашка или химический стакан; стеклянная палочка; конические колбы вместимостью 100, 250 мл; мерные колбы вместимостью 100, 250 мл; бумажный фильтр; обратный холодильник; 1%-ный раствор гексацианоферриата калия (10,5 г красной кровяной соли в 1 л дистиллированной воды); 0,1 М раствор тиосульфата натрия; 2,5 М и 15%-ный растворы гидроксида натрия; 10%-ный раствор соляной кислоты; йодид калия; 30%-ный раствор сульфата цинка; 1%-ный раствор метиленового голубого.
Методика анализа.
- Осуществляют гидролиз и удаление белков (методику см. выше при описании арбитражного метода).
- Определяют редуцирующие сахара (при этом проводят ориентировочное и окончательное титрование). Ориентировочное титрование: в коническую колбу вместимостью 100 мл приливают 10 мл титрованного 1%-ного раствора гексацианоферриата, 2,5 мл 2,5 М раствора гидроксида натрия, каплю 1%-ного раствора метиленового голубого. Затем содержимое колбы нагревают до кипения и к кипящему раствору непрерывно добавляют из бюретки (по 1 капле в 1 с) испытуемый гидролизат до исчезновения синей и появления светло-желтой окраски (наиболее точный результат получают, если на титрование кипящего раствора расходуется 5-6 мл гидролизата).
Окончательное титрование: в коническую колбу вносят 10 мл 1%-ного раствора гексацианоферриата калия, 2,5 мл 2,5 М раствора гидроксида натрия, каплю 1%-ного раствора метиленового голубого и гидролизат в объеме, меньшем на 0,2 - 0,3 мл, по сравнению с израсходованным при ориентировочном титровании. Затем содержимое нагревают до кипения и кипятят 1 мин (не допуская бурного кипения). Не прекращая кипения титруют по 1 капле гидролизатом до полного исчезновения синей окраски.
Содержание хлеба рассчитывают по формуле:
x = (10,06 + 0,0175V)K1 * 250 * 0,9 * 100/(m0V * 10 * 48),
где:
х - содержание хлеба, %;
10,06 и 0,0175 - поправочные коэффициенты, установленные эмпирически для 10 мл 1%-ного раствора гексацианоферриата калия;
V - объем гидролизата, израсходованный при окончательном титровании 10 мл 1%-ного раствора гексацианоферриата калия, мл;
K1 - коэффициент пересчета на точно 1%-ный раствор гексацианоферриата калия;
0,9 - коэффициент пересчета на крахмал;
m0 - масса навески, г;
48 - коэффициент пересчета на хлеб (учитывая содержание углеводов в 100 г хлеба).
Определение коэффициента K1. 50 мл 1%-ного раствора гексацианоферриата калия вносят в коническую колбу с притертой пробкой, добавляют 3 г йодида калия, 1,5 г 30%-ного сульфата цинка, смесь взбалтывают и титруют выделившийся йод 0,1 М раствором тиосульфата натрия в присутствии крахмала в качестве индикатора.
Коэффициент пересчета К1 рассчитывают по формуле:
K1 = 0,03202 * V * K / 0,5,
где:
0,03202 - количество гексацианоферриата калия, эквивалентное 1 мл 0,1 М раствора тиосульфата натрия, г;
V - объем 0,1 М раствора тиосульфата натрия, мл;
К - коэффициент пересчета на точно 0,1 М раствор тиосульфата натрия;
0,5 - содержание гексацианоферриата калия в 50 мл 1% -ного раствора, г.
Расхождение между параллельными определениями должно быть не более 0,5%.
Требования к отчету по лабораторной работе. По результатам анализа сделать выводы.
Контрольные вопросы:
- Основные свойства моносахаридов?
- Какие металлы легко восстанавливаются моносахаридами?
- С помощью какой реакции можно распознать кетозы?
- С помощью какой реакции можно распознать гексозы?
- С помощью какой реакции можно распознать крахмал?